Page 16 - Modul Asam Basa Kelas XI
P. 16
Sifat kuat atau lemah dari asam dapat diketahui dengan alat uji
+
elektrolit. Asam kuat adalah asam yang mudah melepaskan ion H di
dalam air dan mengalami ionisasi total. Sedangkan asam lemah adalah
asam yang terionisasi sebagian di dalam air, sesuai dengan derajat
+
disosiasinya. Berdasarkan jumlah ion H yang dilepaskan, asam
dikelompokkan sebagai berikut.
+
a) Asam monoprotik, yaitu asam yang melepaskan satu ion H jika
dilarutkan dalam air. Contoh: HCl, HNO3, dan HBr.
+
b) Asam diprotik, yaitu asam yang melepaskan dua ion H jika dilarutkan
dalam air. Contoh: H2SO4, H2SO3, dan H2CO3.
c) Asam triprotik atau poliprotik, yaitu asam yang melepaskan tiga ion
+
H jika dilarutkan dalam air. Contoh: H3PO4, dan H3AsO4.
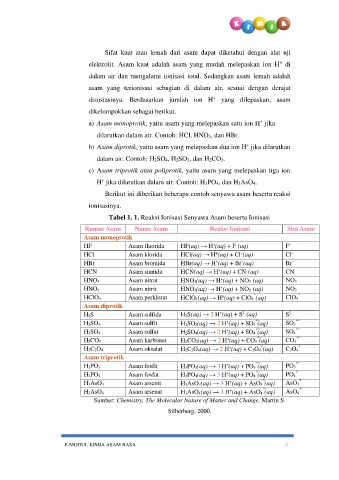
Berikut ini diberikan beberapa contoh senyawa asam beserta reaksi
ionisasinya.
Tabel 1. 1. Reaksi Ionisasi Senyawa Asam beserta Ionisasi
Rumus Asam Nama Asam Reaksi Ionisasi Sisa Asam
Asam monoprotik
–
HF Asam fluorida HF(aq) → H (aq) + F (aq) F –
+
+
HCl Asam klorida HCl(aq) → H (aq) + Cl (aq) Cl
–
–
+
–
HBr Asam bromida HBr(aq) → H (aq) + Br (aq) Br
–
–
–
+
HCN Asam sianida HCN(aq) → H (aq) + CN (aq) CN
–
+
HNO3 Asam nitrat HNO3(aq) → H (aq) + NO3 (aq) NO3 –
–
+
HNO2 Asam nitrit HNO2(aq) → H (aq) + NO2 (aq) NO2 –
– –
+
HClO4 Asam perklorat HClO4(aq) → H (aq) + ClO4 (aq) ClO4
Asam diprotik
2–
+
H2S Asam sulfida H2S(aq) → 2 H (aq) + S (aq) S 2–
2– 2–
+
H2SO3 Asam sulfit H2SO3(aq) → 2 H (aq) + SO3 (aq) SO3
2– 2–
+
H2SO4 Asam sulfat H2SO4(aq) → 2 H (aq) + SO4 (aq) SO4
2– 2–
+
H2CO3 Asam karbonat H2CO3(aq) → 2 H (aq) + CO3 (aq) CO3
2– 2–
+
H2C2O4 Asam oksalat H2C2O4(aq) → 2 H (aq) + C2O4 (aq) C2O4
Asam triprotik
3– 3–
+
H3PO3 Asam fosfit H3PO3(aq) → 3 H (aq) + PO3 (aq) PO3
3– 3–
+
H3PO4 Asam fosfat H3PO4(aq) → 3 H (aq) + PO4 (aq) PO4
3– 3–
+
H3AsO3 Asam arsenit H3AsO3(aq) → 3 H (aq) + AsO3 (aq) AsO3
3– 3–
+
H3AsO4 Asam arsenat H3AsO4(aq) → 3 H (aq) + AsO4 (aq) AsO4
Sumber: Chemistry, The Molecular Nature of Matter and Change, Martin S.
Silberberg, 2000.
E-MODUL KIMIA ASAM BASA 5