Page 47 - Modul Asam Basa Kelas XI
P. 47
2) Hanya ada satu harga konsentrasi untuk masing-masing spesies
dalam larutan, tidak melihat asalnya, dan masing masing harga
konsentrasi harus konsisten dengan semua tetapan ionisasi
dimana harga tersebut berada. (Sebagai contoh, hanya ada satu
+
harga konsentrasi untuk [H3O ] dalam H3PO4(aq), harga ini
dipakai dalam Ka1, Ka2, dan Ka3).
3) Urutan besar kecilnya tetapan ionisasi adalah selalu Ka1 > Ka2 >
Ka3.
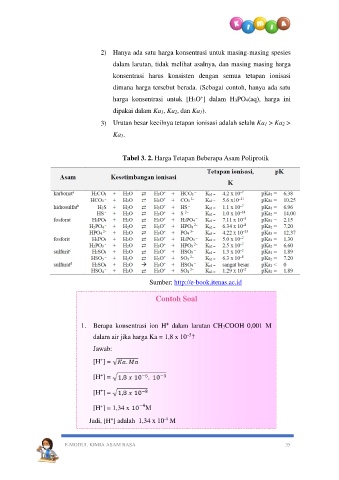
Tabel 3. 2. Harga Tetapan Beberapa Asam Poliprotik
Sumber: http://e-book.itenas.ac.id
Contoh Soal
+
1. Berapa konsentrasi ion H dalam larutan CH3COOH 0,001 M
–5
dalam air jika harga Ka = 1,8 x 10 ?
Jawab:
+
[H ] =
+
[H ] =
+
[H ] =
+
[H ] = 1,34 x M
-4
+
Jadi, [H ] adalah 1,34 x 10 M
E-MODUL KIMIA ASAM BASA 35