Page 101 - Traité de chimie thérapeutique 6 Médicaments antitumoraux
P. 101
4. MOUTARDES À L'AZOTE 57
0 u
o
0 ···:0
EtOOC
0
1J / ,""
~ ,o,
2)EOH,
8 9
EtOOC
NH2
° 11
1/ ~
10
1) POClgou SOC2 HOOC ra.
2) so' N
12 •
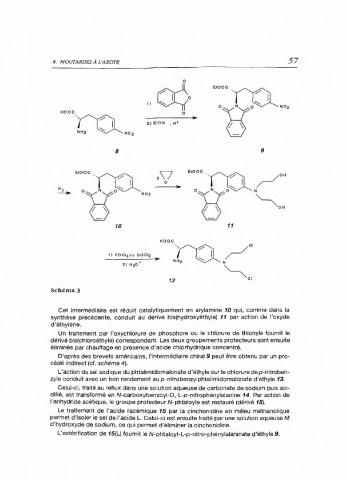
Schéma 3
Cet intermédiaire est réduit catalytiquement en arylamine 10 qui, comme dans la
synthèse précédente, conduit au dérivé bis(hydroxyéthyle) 11 par action de l'oxyde
d'éthylène.
Un traitement par l'oxychlorure de phosphore ou le chlorure de thionyle fournit le
dérivé bis(chloroéthyle) correspondant. Les deux groupements protecteurs sont ensuite
éliminés par chauffage en présence d'acide chlorhydrique concentré.
D'après des brevets américains, l'intermédiaire chiral 9 peut être obtenu par un pro-
cédé indirect (cf. schéma 4).
L'action du sel sodique du phtalimidomalonate d'éthyle sur le chlorure de p-nitroben-
zyle conduit avec un bon rendement au p-nitrobenzylphtalimidomalonate d'éthyle 13.
Celui-ci, traité au reflux dans une solution aqueuse de carbonate de sodium puis aci-
difié, est transformé en N-carboxybenzoyl-D, L-p-nitrophénylalanine 14. Par action de
l'anhydride acétique, le groupe protecteur N-phtaloyle est restauré (dérivé 15).
Le traitement de l'acide racémique 15 par la cinchonldine en milieu méthanolique
permet d'isoler le sel de l'acide L. Celui-ci est ensuite traité par une solution aqueuse M
d'hydroxyde de sodium, ce qui permet d'éliminer la cinchonidine.
L'estérification de 15(L) fournit le N-phtaloyl-L-p-nitro-phénylalaninate d'éthyle 9.