Page 192 - Traité de Chimie Thérapeutique 2 : Médicaments Antibiotiques
P. 192
182 MÉDICAMENTS ANTIBIOTIQUES
CH3 A• H Y » S< NH-CO-CH,
H......
y
RO R = SO,H y. S ~ NH-CO-CH 3
N
O"
\
COOH R • SOH Y .. SO NH-CO--CH,
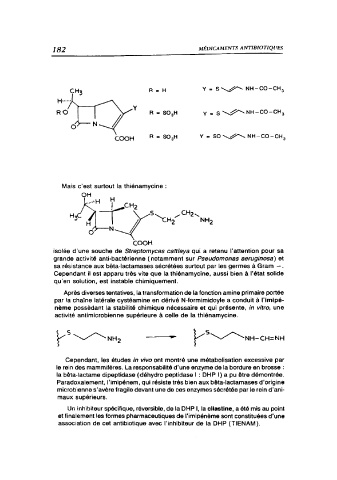
Mais c'est surtout la thiénamycine :
H
OH
<.y-.
COOH
isolée d'une souche de Streptomyces cattleya qui a retenu l'attention pour sa
grande activité anti-bactérienne ( notamment sur Pseudomonas aeruginosa) et
sa résistance aux bêta-lactamases sécrétées surtout par les germes à Gram -.
Cependant il est apparu très vite que la thiénamycine, aussi bien à l'état solide
qu'en solution, est instable chimiquement.
Après diverses tentatives, la transformation de la fonction amine primaire portée
par la chaîne latérale cystéamine en dérivé N-formimidoyle a conduit à l'imipé-
nème possédant la stabilité chimique nécessaire et qui présente, in vitro, une
activité antimicrobienne supérieure à celle de la thiénamycine.
>-»
Cependant, les études in vivo ont montré une métabolisation excessive par
le rein des mammifères. La responsabilité d'une enzyme de la bordure en brosse :
la bêta-lactame dipeptidase (déhydro peptidase 1 : DHP 1) a pu être démontrée.
Paradoxalement, l'imipénem, qui résiste très bien aux bêta-lactamases d'origine
microbienne s'avère fragile devant une de ces enzymes sécrétée par le rein d'ani-
maux supérieurs.
Un inhibiteur spécifique, réversible, de la DHP I, la cllastine, a été mis au point
et finalement les formes pharmaceutiques de l'imipénème sont constituées d'une
association de cet antibiotique avec l'inhibiteur de la DHP (TIENAM).