Page 252 - Traité de Chimie Thérapeutique 2 : Médicaments Antibiotiques
P. 252
242 MÉDICAMENTS ANTIBIOTIQUES
1.3. MÉCANISME D'ACTION
Le mécanisme réactionnel des bêta-lactamases face aux antibiotiques est tout
à fait comparable à celui décrit plus haut pour le mode d'action des antibiotiques
à structure bêta-lactame vis-à-vis des enzymes conduisant à la biosynthèse des
parois.
A titre d'exemple, le mécanisme avec l'acide sulfopénicillanique ( sulbactam
utilisable en association) pourrait être le suivant ( figure 1 ).
0 \7o ,,"e·
ce s ~ 0t N--l• -0■9 (N _ ,,,,~
'
l"'I~
~so2
_
/
o } ~ o (j ' o 1 •• "coo
O-H COOH I COOH -Ser - H
l H -Ser -. H
_ Ser
70 0
OH
- Ser -
@
O
802
-
- o.c / < Désacylation
»
/
o l - ç, l ···cooH
1 H '; Isomérisation
- Ser -
0
énamine
O-C = HN- @ ( ll-am,no. acryiate)
1
0
1
-- Set -
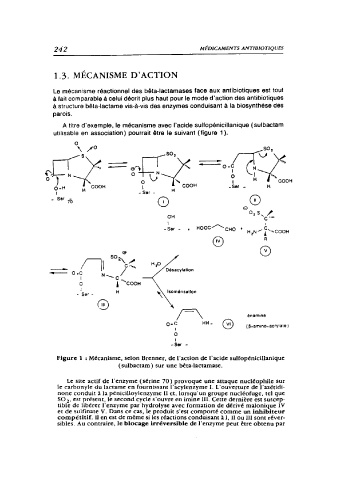
Figure 1 :Mécanisme, selon Brenner, de l'action de l'acide sulfopénicillanique
( sulbactam) sur une bêta-lactamase.
Le site actif de l'enzyme ( sérine 70) provoque une attaque nucléophile sur
le carbonyle du lactame en fournissant l'acylenzyme 1. L'ouverture de l'azétidi-
none conduit à la pénicilloylcnzyme II et, lorsqu'un groupe nucléofuge, tel que
SO , est présent, le second cycle s'ouvre en imine Ill. Cette dernière est suscep-
2
tible de libérer l'enzyme par hydrolyse avec formation de dérivé malonique IV
et de sulfinate V. Dans ce cas, le produit s'est comporté comme un inhibiteur
compétitif. Il en est de même si les réactions conduisant à I, Il ou Ill sont réver-
sibles. Au contraire, le blocage irréversible de l'enzyme peut être obtenu par