Page 281 - Traité de Chimie Thérapeutique 2 : Médicaments Antibiotiques
P. 281
271
7. LA FOSFOMYCINE
de chiralité (SS). Un traitement par le bromoacétamide (CH,CONHBr) à 15°C,
en présence d'eau conduit à une réaction d'addition stéréosélective trans ; on
obtient ainsi la bromhydrine 15 de géométrie SRSS de manière largement majo-
ritaire devant le dérivé 15' RSSS. La cristallisation sous forme d'amide isopropy-
lique permet la purification du dérivé 15. Ce dernier est ensuite soumis à l'action
d'une solution aqueuse d'acide bromhydrique qui libère la bromhydrine phospho-
nique 16 qui, sous l'action de CH ONa, conduit à la cyclisation stéréospécifique
3
en sel de sodium de fosfomycine.
HO (S) COOMe
H H
C==C .--··'
+ a C
HOkCOOMo "'Cl
o
11 12
H. .H H.. .H COOMe
--....,P,J2s1
c
S
l
·····c = c······ o ISJ... COOMe- ··c =c··· o..._~si
M./ Me~ '-..p / 'oH
0 0 COOMe O O H COOMe
13 14
H (S) Br-
• ·c-c······ .H COOMe
I
~"l 6«,"""a 15
a,eo
• r
H20.15"C OH COOMe
OH
a,, (s) • COOMe 15'
H •.,.. I
C -c ····
,-OS)s»
a gI o»
COOMe
H I' Br
• 1 • H
15 c-c·····
• 79%
>
o
Q_./ p
1 h
O
H --°""
OH
16
Mar > >, ooNa@
H..
H
cc
1/ .......
O ONa
fosfomycine
(sel de Na)
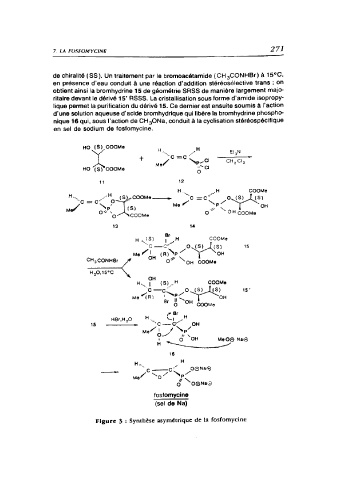
Figure 3 : Synthèse asymétrique de la fosfomycine