Page 330 - Traité de Chimie Thérapeutique 4 Médicaments en relation avec des systèmes hormonaux
P. 330
4. LES NORMOLIPEMIANTS 291
Les principales étapes de cette synthèse sont :
1) l'élaboration du squelette hexahydronaphtalénique du composé 93 à configura
tion 1S,2S,6S,8S,8aR via la lactone 85,
2) la C1-homologation suivie d'une hétérocyclisation conduisant à la 2,3-dihydro-y-
pyrone 97,
3) sa transformation en un acétal 101 et enfin
4) l'accès au squelette hexahydronaphtalénique de la pravastatine 109, via
l'époxyde 105.
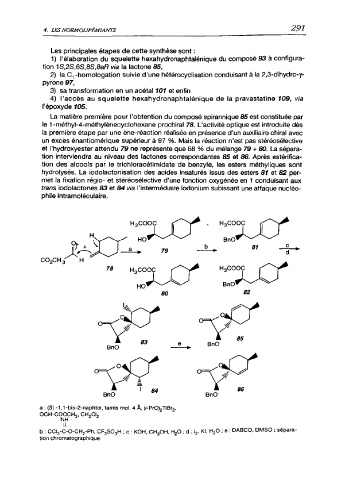
La matière première pour l’obtention du composé spirannique 85 est constituée par
le 1 -méthyl-4-méthylènecyclohexane prochiral 78. L'activité optique est introduite dès
la première étape par une ène-réaction réalisée en présence d'un auxiliaire chiral avec
un excès énantiomérique supérieur à 97 %. Mais la réaction n'est pas stéréosélective
et l'hydroxyester attendu 79 ne représente que 68 % du mélange 79 + 80. La sépara
tion interviendra au niveau des lactones correspondantes 85 et 86. Après estérifica
tion des alcools par le trichloracétimidate de benzyle, les esters méthyliques sont
hydrolysés. La iodolactonisation des acides insaturés issus des esters 81 et 82 per
met la fixation régio- et stéréosélective d’une fonction oxygénée en 1 conduisant aux
trans iodolactones 83 et 84 via l’intermédiaire iodonium subissant une attaque nucléo-
phile intramoléculaire.
a : (S) -1,1-bis-2-naphtol, tamis mol. 4 A, (/'-PrO)2TiBr2,
OCH-COOCHo, CH-CI,
NH 3 22
II
b : CCI3-C-O-CH2-Ph, CF3SO3H ; c : KOH, CH3OH, H2O ; d : l2, Kl, H2O ; e : DABCO. DMSO ; sépara
tion chromatographique.