Page 333 - Traité de Chimie Thérapeutique 4 Médicaments en relation avec des systèmes hormonaux
P. 333
294 MÉDICAMENTS ENRELA TION A VEC DES SYSTÈMES HORMONAUX
R1 R3 R4' N°
Ac Ac H 99
H H H 100
H t-BuPh2Si t-BuPh2Si 101
m : H3CO-CH2 PPh3, Cl", t-BuOK, THF
n : Bu4NF, THF ; Ac2O, DMAP, pyridine
o : acide para-toluènesulfonique, acétone, H2O
p : TiCI4, CH2CI2, 96 ; CF3COOH, THF (diastéréoisomères : 92 :8)
q : MeOH, Et3N
r : (sec-Bu)3BHU, THF ; H2O2
s : KOH, MeOH
t : t-BuPh2SiCI, imidazole, DMF
ch-co-chA
// 3
, t-BuO2H
ch3
2
v : (+)-(S)-(CH3-CH2-CH-CO)2O, pyridine, DMAP
ch3
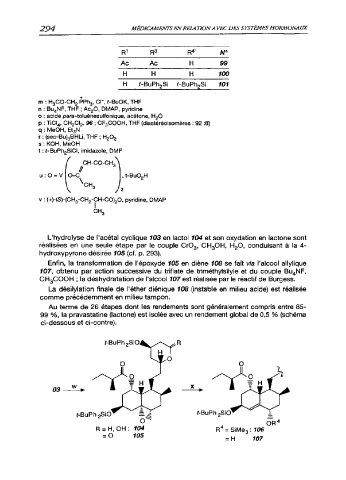
L'hydrolyse de l'acétal cyclique 103 en lactol 104 et son oxydation en lactone sont
réalisées en une seule étape par le couple CrO3, CH3OH, H2O, conduisant à la 4-
hydroxypyrone désirée 105 (cf. p. 293).
Enfin, la transformation de l'époxyde 105 en diène 108 se fait via l'alcool allylique
107, obtenu par action successive du triflate de triméthylsilyle et du couple Bu4NF,
CH3COOH ; la déshydratation de l'alcool 107 est réalisée par le réactif de Burgess.
La désilylation finale de l’éther diénique 108 (instable en milieu acide) est réalisée
comme précédemment en milieu tampon.
Au terme de 26 étapes dont les rendements sont généralement compris entre 85
99 %, la pravastatine (lactone) est isolée avec un rendement global de 0,5 % (schéma
ci-dessous et ci-contre).