Page 804 - Traité de Chimie Thérapeutique 4 Médicaments en relation avec des systèmes hormonaux
P. 804
19 LA VITAMINE A ET LES RÉTINOÏDES 765
Cette réaction doit être réalisée dans du chloroforme exempt de toute trace d'étha
nol qui, agissant comme nucléophile, s'additionne sur le carbénium et fait disparaître
la coloration.
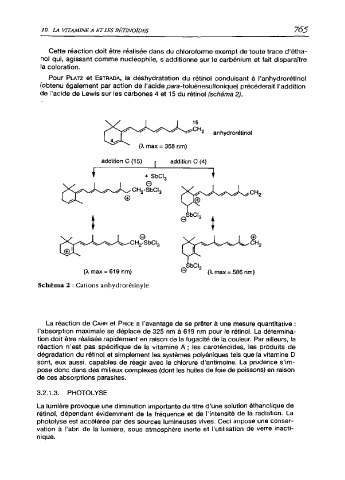
Pour Platz et Estrada, la déshydratation du rétinol conduisant à l'anhydrorétinol
(obtenu également par action de l'acide para-toluènesulfonique) précéderait l'addition
de l'acide de Lewis sur les carbones 4 et 15 du rétinol (schéma 2).
Schéma 2 : Cations anhydrorétinyle
La réaction de Carr et Price a l'avantage de se prêter à une mesure quantitative :
l'absorption maximale se déplace de 325 nm à 619 nm pour le rétinol. La détermina
tion doit être réalisée rapidement en raison de la fugacité de la couleur. Par ailleurs, la
réaction n'est pas spécifique de la vitamine A ; les caroténoïdes, les produits de
dégradation du rétinol et simplement les systèmes polyéniques tels que la vitamine D
sont, eux aussi, capables de réagir avec le chlorure d'antimoine. La prudence s'im
pose donc dans des milieux complexes (dont les huiles de foie de poissons) en raison
de ces absorptions parasites.
3.2.1.3. PHOTOLYSE
La lumière provoque une diminution importante du titre d'une solution éthanolique de
rétinol, dépendant évidemment de la fréquence et de l'intensité de la radiation. La
photolyse est accélérée par des sources lumineuses vives. Ceci impose une conser
vation à l'abri de la lumière, sous atmosphère inerte et l'utilisation de verre inacti-
nique.