Page 381 - Traité de Chimie Thérapeutique 2 : Médicaments Antibiotiques
P. 381
10. LES MACROL.IDES ET ANTIBIOTIQUES APPARENTÉS 371
de la stabilité en milieu gastrique et de la résorption intestinale sans altération
des propriétés antibactériennes.
En effet, l'oxime de l'érythromycine est stable en milieu acide, la formation
des cétals internes étant empêchée, mais son activité antibiotique est affaiblie.
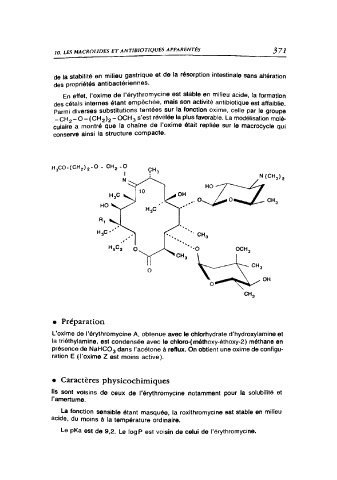
Parmi diverses substitutions tentées sur la fonction oxime, celle par le groupe
-CH,--O-(CH,),-OCH, s'est révélée la plus favorable. La modélisation molé-
culaire a montré que la chaîne de l'oxime était repliée sur le macrocycle qui
conserve ainsi la structure compacte.
HCO-(CH,),-O - CH,-O
1 N(CH,),
N
Ez
OH .. o o CH,
..
0
OH
• Préparation
L'oxime de l'érythromycine A, obtenue avec le chlorhydrate d'hydroxylamine et
la triéthylamine, est condensée avec le chloro-(méthoxy-éthoxy-2) méthane en
présence de NaHC0 dans l'acétone à reflux. On obtient une oxime de configu-
3
ration E (l'oxime Z est moins active).
• Caractères physicochimiques
Ils sont voisins de ceux de l'érythromycine notamment pour la solubilité et
l'amertume.
La fonction sensible étant masquée, la roxithromycine est stable en milieu
acide, du moins à la température ordinaire.
Le pKa est de 9,2. Le log p est voisin de celui de l'érythromycine.