Page 182 - Traité de chimie thérapeutique 6 Médicaments antitumoraux
P. 182
138 MEDICAMENTSINDUISANT DES MODIFICATIONS COVALENTES DEL 'ADN
6.1. ACTIVATION MONOFONCTIONNELLE EN C 1
La différence entre les potentiels d'oxydoréduction de 15 et de 2est telle qu'en présence
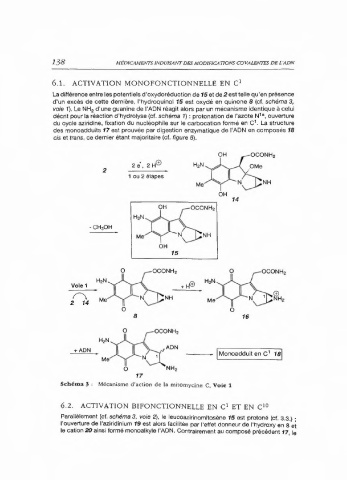
d'un excès de cette dernière, l'hydroquinol 15 est oxydé en quinone 8 (cf. schéma 3,
voie 1). Le NH, d'une guanine de l'ADN réagit alors par un mécanisme identique à celui
décrit pour la réaction d'hydrolyse (cf. schéma 1): protonation de l'azote Nia, ouverture
du cycle aziridine, fixation du nucléophile sur le carbocation formé en ci. La structure
des monoadduits 17 est prouvée par digestion enzymatique de l'ADN en composés 18
cis et trans, ce dernier étant majoritaire (cf. figure 8).
OH
av J_y9o»
26,2@ OMe
2
1 ou 2 étapes
MeN
IINH
N
OH
14
OH 2
H N, À --(OCONH
2
we N.NH
I.
OH
15
,
Voie 1
2 14
8 16
0 OCONH2
% ADN
HAN
+ADN 1 Monoadduit en ci 1sJ
Me - - - -
O NH,
17
Schéma 3 : Mécanisme d'action de la mitomycine C, Voie 1
6.2. ACTIVATION BIFONCTIONNELLE EN C' ET EN CO
Parallèlement (cf. schéma 3, voie 2), le leucoazirinomitosène 15 est protoné (cf. 3.3.) ;
l'ouverture de l'aziridinium 19 est alors facilitée par l'effet donneur de l'hydroxy en a et
le cation 20 ainsi formé monoalkyle l'ADN. Contrairement au composé précédent 17, le