Page 185 - Traité de chimie thérapeutique 6 Médicaments antitumoraux
P. 185
8. MITOMYCINE C 141
L'intermédiaire 21 évolue différemment selon l'environnement :
- si une deuxième guanine se trouve à proximité en bonne position sur l'un ou l'autre
brin d'ADN, un adduit bifonctionnel 22 est formé. Le pontage intrabrin concerne deux
guanines consécutives sur un même brin ; la bisalkylation interbrin se fait exclusive-
ment sur des séquences 5'CpG3'. Ces adduits bifonctionnels interbrin et intrabrin
peuvent être isolés puis caractérisés après digestion enzymatique et oxydation qui les
transforment en composés 23 et 24 dont les structures sont indiquées sur la figure 8 ;
- en l'absence d'une deuxième guanine en bonne position (cf. schéma 3, voie 3), le site
électrophile en 10 réagit avec une molécule d'eau pour conduire à un monoadduit
décarbamoylé 25 caractérisée par isolement de 26 (cf. figure 9).
Le fait que les alkylations aient lieu sur le NH, des guanines et non en N' montre que
la mitomycine est dans le petit sillon de l'ADN.
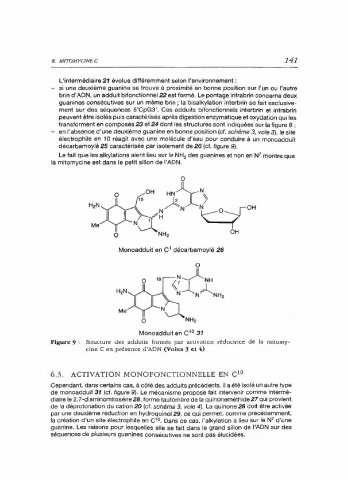
Monoadduit en C' décarbamoylé 26
0
0
Monoadduit en ç' 31
Figure 9 : Structure des adduits formés par activation réductrice de la mitomy-
cine C en présence d'ADN (Voies 3 et 4)
6.3. ACTIVATION MONOFONCTIONNELLE EN CIO
Cependant, dans certains cas, à côté des adduits précédents, il a été isolé un autre type
de monoadduit 31 (cf. figure 9). Le mécanisme proposé fait intervenir comme intermé-
diaire le 2,7-diaminomitosène 28, forme tautomère de la quinoneméthide 27 qui provient
de la déprotonation du cation 20 (cf. schéma 3, voie 4). La quinone 28 doit être activée
par une deuxième réduction en hydroquinol 29, ce qui permet, comme précédemment,
la création d'un site électrophile en C'. Dans ce cas, l'alkylation a lieu sur le N' d'une
guanine. Les raisons pour lesquelles elle se fait dans le grand sillon de l'ADN sur des
séquences de plusieurs guanines consécutives ne sont pas élucidées.