Page 803 - Traité de chimie thérapeutique 6 Médicaments antitumoraux
P. 803
39. AGENTS RADIO Er CHJMJOSENSIBIUSANTS 761
3.1.1. Voie d'accès
Une des difficultés majeures est le contrôle de la régiosélectivité de l'oxydation des azo-
tes de la benzotriazine (schéma 1). Il est préférable de préparer 9 (déjà N-oxydé en 1) et
de peroxyderensuite le N: la 1-oxy-benzo[1,2,4]-triazin-3-yl-amine9 est préparée (avec
passage par l'intermédiaire 8) à partir de l'ortho-nitraniline 6 par action de cyanamide 7.
La tirapazamine est obtenue (rdt 40 %) par action de H,O, en milieu acétique à 45-50 °C.
Une autre approche (SNG et LEY) consiste à préparer directement un dianion 11 dioxy-
géné en 1,4 par action du cyanamide disodique sur le benzofuroxane 10, puis à pratiquer
une hydrolyse acétique (rdt : 80 %).
i
(X NO, NH " 1) 100 •c (X
"
+
C
'i» 2) HCI conc. Nti""'\IH
a 9
j
4s-so •c
tlrapazamlno ~ H 0@
3
•
N, e I L e
o: "_- -,>
w <
e " , i
10 e
Schéma 1 : Voies d'accès à la tirapazamine
3.1.2. Caractéristiques physicochimiques
Poudre cristalline orange, F •c = 220 (acide acétique).
- Spectre IR: bandes principales à 3 400, 3 250, 3 200, 1 630-1 640 cm'
- Spectre UV, éthanol: À. max (log e):272 nm (4,24); 474 nm (3,52); inflexion à226 nm.
- Spectre de masse (IE) ; m/z (%) : 118(100) 162 (14), 136 (34), 78 (16)...
1
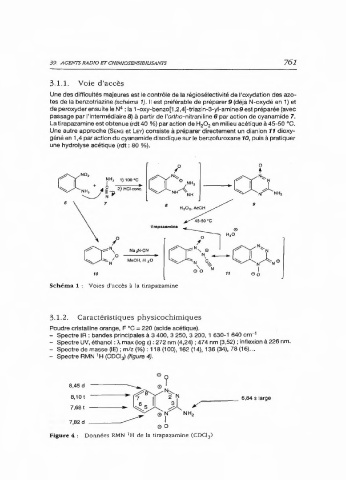
- Spectre RMN H (CDCl:i) (figure 4).
8,45 d
8,10t
7,68t
7,82d
Figure 4: Données RMN 'H de la tirapazamine (COCl )
3