Page 205 - Traité de Chimie Thérapeutique 2 : Médicaments Antibiotiques
P. 205
4.LES THIÉNAMYCINES 195
HN
H
• L:;@
COOH COOH
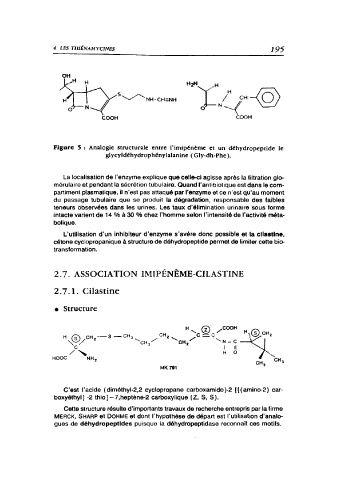
Figure 5 : Analogie structurale entre l'imipénème et un déhydropeptide le
glycyldéhydrophénylalanine ( Gly-dh-Phe ).
La localisation de l'enzyme explique que celle-ci agisse après la filtration glo-
mérulaire et pendant la sécrétion tubulaire. Quand l'antibiotique est dans le com-
partiment plasmatique, il n'est pas attaqué par l'enzyme et ce n'est qu'au moment
du passage tubulaire que se produit la dégradation, responsable des faibles
teneurs observées dans les urines. Les taux d'élimination urinaire sous forme
intacte varient de 14 % à 30 % chez l'homme selon l'intensité de l'activité méta-
bolique.
L'utilisation d'un inhibiteur d'enzyme s'avère donc possible et la cilastine,
cétone cyclopropanique à structure de déhydropeptide permet de limiter cette bio-
transformation.
2.7. ASSOCIATION IMIPÉNÈME-CILASTINE
2.7.1. Cilastine
• Structure
C'est l'acide (diméthy!-2,2 cyclopropane carboxamido)-2 [[(amin0-2) car-
boxyéthyl] -2 thio] --7,heptène-2 carboxylique (Z, S, s).
Cette structure résulte d'importants travaux de recherche entrepris par la firme
MERCK, SHARP et DOHME et dont l'hypothèse de départ est l'utilisation d'analo-
gues de déhydropeptldes puisque la déhydropeptidase reconnaît ces motifs.