Page 131 - Chimie organique - cours de Pau 2- Brigitte Jamart
P. 131
Partie 1 ■ Chimie organique générale
'ouesin5.c
Ayant effectué la réaction RBr+OH ROH+Br avec deux dérivés bromés différents RBr et R'Br,
on a trouvé deux lois de vitesse différentes: v= k[RBr][OH] et V= K' [R'Br]. Laquelle de ces deux
réactions peut ne comporter qu'une étape, et laquelle en comporte-t-elle nécessairement plus
d'une?
5.2.4 La catalyse
Un catalyseur est un corps qui, par sa présence dans un système capable d'évoluer chimiquement, accé-
lère la transformation sans participer à son bilan et, en général, sans être lui-même modifié. Il peut donc
«resservir» et il n'y a pas de rapport stœchiométrique entre sa masse et celle des produits formés.
Contrairement à une élévation de température, un catalyseur n'apporte pas d'énergie. Mais sa
présence abaisse l'énergie d'activation de la transformation et, toutes choses égales par ailleurs
(température, concentrations des réactifs) la transformation est donc rendue plus rapide, puisque la
proportion de molécules aptes à réagir est plus grande.
Ce résultat est obtenu par une modification du « chemin réactionnel » pouvant aller jusqu'à
remplacer une réaction en une étape par une autre quis' effectue en plusieurs étapes (fig. 5.3).
Exemple
La réaction
RCI+OH ROH+CI
est relativement lente, mais elle s'effectue beaucoup plus rapidement en présence d'ions iodure 1-,
apportés par une addition d'iodure de sodium Nal dans le milieu réactionnel. Dans ces conditions, elle
s'effectue en deux étapes :
1)RCI+I RI+CI
2) RI+OH ROH+I
et il se trouve que chacune de ces deux réactions a une énergie d'activation inférieure à celle de la
réaction directe non catalysée. En présence de 1-, le profil de la réaction, au lieu d'être du type «A»
(fig. 5.3) est du type «C»;le dérivé iodé RI est l'intermédiaire de la réaction catalysée et il correspond
au «creux» du profil.
î
Ea-T_,_--
E'
a
1
s
Coordonnées da la ni
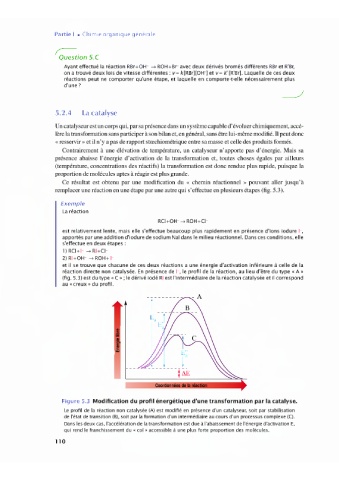
Figure 5.3 Modification du profil énergétique d'une transformation par la catalyse.
Le profil de la réaction non catalysée (A) est modifié en présence d'un catalyseur, soit par stabilisation
de l'état de transition (B), soit par la formation d'un intermédiaire au cours d'un processus complexe (C).
Dans les deux cas, l'accélération de la transformation est due à l'abaissement de l'énergie d'activation E,
qui rend le franchissement du «col» accessible à une plus forte proportion des molécules.
110