Page 154 - Traité de Chimie Thérapeutique 4 Médicaments en relation avec des systèmes hormonaux
P. 154
2. MÉDICAMENTS DU DIABÈTE SUCRÉ UTILISABLES PAR VOIE ORALE 115
2.1.1.1. VOIE D'ACCÈS
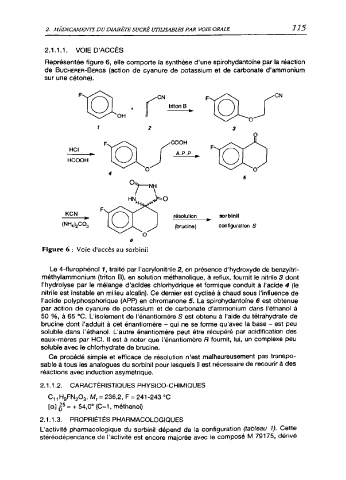
Représentée figure 6, elle comporte la synthèse d'une spirohydantoïne par la réaction
de Bucherer-Bergs (action de cyanure de potassium et de carbonate d'ammonium
sur une cétone).
Figure 6 : Voie d'accès au sorbinil
Le 4-flurophénol 1, traité par l'acrylonitrile 2, en présence d'hydroxyde de benzyltri-
méthylammonium (triton B), en solution méthanolique, à reflux, fournit le nitrile 3 dont
l'hydrolyse par le mélange d'acides chlorhydrique et formique conduit à l'acide 4 (le
nitrile est instable en milieu alcalin). Ce dernier est cyclisé à chaud sous l'influence de
l'acide polyphosphorique (APP) en chromanone 5. La spirohydantoïne 6 est obtenue
par action de cyanure de potassium et de carbonate d’ammonium dans l'éthanol à
50 %, à 65 °C. L'isolement de l'énantiomére S est obtenu à l'aide du tétrahydrate de
brucine dont l'adduit à cet énantiomère - qui ne se forme qu'avec la base - est peu
soluble dans l'éthanol. L'autre énantiomère peut être récupéré par acidification des
eaux-mères par HCl. Il est à noter que l'énantiomère R fournit, lui, un complexe peu
soluble avec le chlorhydrate de brucine.
Ce procédé simple et efficace de résolution n'est malheureusement pas transpo
sable à tous les analogues du sorbinil pour lesquels il est nécessaire de recourir à des
réactions avec induction asymétrique.
2.1.1.2. CARACTÉRISTIQUES PHYSICO-CHIMIQUES
C,, HgFN2O3, Mr = 236,2, F = 241 -243 °C
[a] q5 = + 54,0° (C=1, méthanol)
2.1.1.3. PROPRIÉTÉS PHARMACOLOGIQUES
L'activité pharmacologique du sorbinil dépend de la configuration (tableau 1). Cette
stéréodépendance de l'activité est encore majorée avec le composé M 79175, dérivé