Page 166 - Efavirenz WHO PQ: A case study of a public-private collaboration
P. 166
Efavirenz WHO PQ: กรณีศึกษาความร่วมมือรัฐ-เอกชน ในการถ่ายทอดเทคโนโลยีการผลิตและควบคุมคุณภาพ | 148
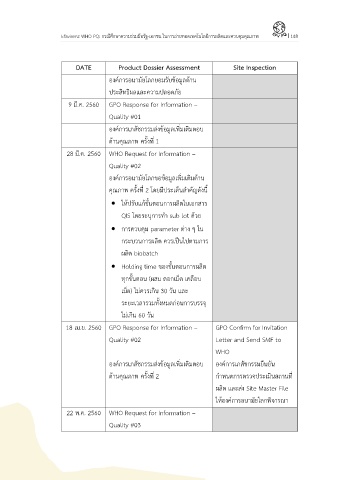
DATE Product Dossier Assessment Site Inspection
องค์การอนามัยโลกยอมรับข้อมูลด้าน
ประสิทธิผลและความปลอดภัย
9 มี.ค. 2560 GPO Response for Information –
Quality #01
องค์การเภสัชกรรมส่งข้อมูลเพิ่มเติมตอบ
ด้านคุณภาพ ครั้งที่ 1
28 มี.ค. 2560 WHO Request for Information –
Quality #02
องค์การอนามัยโลกขอข้อมูลเพิ่มเติมด้าน
คุณภาพ ครั้งที่ 2 โดยมีประเด็นส าคัญดังนี้
ให้ปรับแก้ขั้นตอนการผลิตในเอกสาร
QIS โดยระบุการท า sub lot ด้วย
การควบคุม parameter ต่าง ๆ ใน
กระบวนการผลิต ควรเป็นไปตามการ
ผลิต biobatch
Holding time ของขั้นตอนการผลิต
ทุกขั้นตอน (ผสม ตอกเมด เคลือบ
็
เม็ด) ไม่ควรเกิน 30 วัน และ
่
ระยะเวลารวมทั้งหมดกอนการบรรจุ
ไม่เกิน 60 วัน
18 เม.ย. 2560 GPO Response for Information – GPO Confirm for Invitation
Quality #02 Letter and Send SMF to
WHO
องค์การเภสัชกรรมส่งข้อมูลเพิ่มเติมตอบ องค์การเภสัชกรรมยืนยัน
ด้านคุณภาพ ครั้งที่ 2 ก าหนดการตรวจประเมินสถานที่
ผลิต และส่ง Site Master File
ให้องค์การอนามัยโลกพิจารณา
22 พ.ค. 2560 WHO Request for Information –
Quality #03