Page 464 - Traité de Chimie Thérapeutique 4 Médicaments en relation avec des systèmes hormonaux
P. 464
425
7 ESTROGÎ-NES
2.2.1. Hémisynthèse
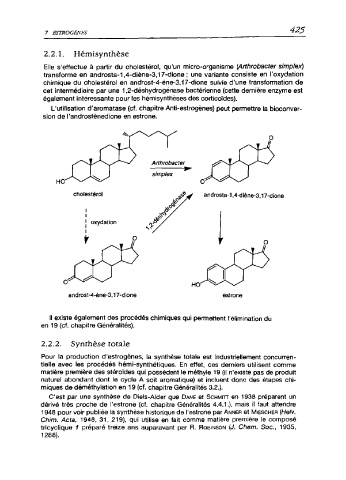
Elle s'effectue à partir du cholestérol, qu'un micro-organisme {Arthrobacter simplex)
transforme en androsta-1,4-diène-3,17-dione ; une variante consiste en l’oxydation
chimique du cholestérol en androst-4-ène-3,17-dione suivie d'une transformation de
cet intermédiaire par une 1,2-déshydrogénase bactérienne (cette dernière enzyme est
également intéressante pour les hémisynthèses des corticoïdes).
L'utilisation d'aromatase (cf. chapitre Anti-estrogènes) peut permettre la bioconver
sion de l’androstènedione en estrone.
Il existe également des procédés chimiques qui permettent l’élimination du
en 19 (cf. chapitre Généralités).
2.2.2. Synthèse totale
Pour la production d'estrogènes, la synthèse totale est industriellement concurren
tielle avec les procédés hémi-synthétiques. En effet, ces derniers utilisent comme
matière première des stéroïdes qui possèdent le méthyle 19 (il n'existe pas de produit
naturel abondant dont le cycle A soit aromatique) et incluent donc des étapes chi
miques de déméthylation en 19 (cf. chapitre Généralités 3.2.).
C'est par une synthèse de Diels-Alder que Dans et Schmitt en 1938 préparent un
dérivé très proche de l'estrone (cf. chapitre Généralités 4.4.1.), mais il faut attendre
1948 pour voir publiée la synthèse historique de l'estrone par Anner et Miescher (Helv.
Chim. Acta, 1948, 31, 219), qui utilise en fait comme matière première le composé
tricyclique 1 préparé treize ans auparavant par R. Robinson (J. Chem. Soc., 1935,
1288).